重组人血管内皮抑素联合化疗治疗胃癌腹膜转移的临床研究
重组人血管内皮抑素联合化疗治疗胃癌腹膜转移的临床研究
蔡铭泉④李毅斌④ 汤玮玮④李晓虹①
【摘要】目的:观察重组人廊管内皮抑素注射液(恩度)联合化疗治疗胃癌腹膜转移的有效性和安全性。方法:选取70例胃癌腹膜转移的患者,随机分为研究组∞=36)和对照组m=34)。研究方案:两组均接受多西他赛75 mg/1T12静脉化疗,替吉奥胶囊(1.25 II12<体表面积<1.5 1112,50mg/次;体表面积≥1.5 1112,60 mg/次,2次/d;连续14 d)口服,同时顺40 mg/mz腹腔灌注化疗。研究组在顺铂腹腔灌注前3d联合恩度60 mg/次,腹腔灌注第1、3天。评价不良反应,每2个周期评价治疗效果,化疗直至疾病进展或毒性不能耐受,多治疗6个周期。结果:两组均无完全缓解患者,研究组部分缓解率25.0%(9/36),疾病稳定率55.6%(20/36),疾病控制率80.6%(29/36),对照组部分缓解率17.6%(6/34),疾病稳定率32.4%(1 l/34),疾病控制率50.0%(17/34),研究组疾病控制率高于对照组,差异有统计学意义(P=0.007)。研究组中位无进展生存时间、巾位总生存时间均优于对照组,差异均有统计学意义(P=0.009、0.023)。两组各不良反应发生率比较,差异均无统计学意义(P>0.05),均无化疗相关死亡。结论:恩度联合化疗可提高治疗胃癌腹膜转移的效果,延长生存期,不增加明显不良反应。
【关键词】重组人血管内皮抑素; 腹腔灌注化疗; 胃癌; 腹膜转移癌
胃癌是常见恶性肿瘤之一,在全球发病率位居第四,在亚太地区胃癌死亡率仅次于肺癌和肝癌,位列恶性肿瘤的第三位。晚期胃癌易发生腹膜转移合并恶性腹腔积液,其治疗效果差,生存期短。而针对胃癌腹腔转移目前缺乏有效治疗方案,有研究表明恶性腹水形成的主要原因为腹腔内新生血管的形成和微血管通透性的增加,血管内皮生长因子是介导新生血管形成及血管通透性增加的关键调节因素[1]。重组人血管内皮抑制素注射液(恩度)具有抑制肿瘤血管生成的作用,笔者所在科采用恩度联合顺铂腹腔灌注及多西他赛联合替吉奥治疗晚期胃癌患者,取得较好临床效果,现报告如下。
1 资料与方法
1.1 -般资料
抽取笔者所在医院2014年1月-2016年12月收治的晚期胃癌患者70例,男41例,女29例,年龄25—70岁,人选标准:所有患者均经病理组织学或细胞学确诊;符合2010年版美国癌症联合委员会(AJCC)TNM分期中Ⅳ期胃腺癌标准,腹水细胞学或腹膜活检证实腹膜腔转移;美国东部肿瘤协作组(ECOG)体力状态(Ps)评分0—2分;至少有一个可评价病灶(根据RECEST版本1.1标准评估):CT或MR检测病灶大直径≥l cm;无重要器官功能障碍,血常规及肝肾功能基本正常;预计生存期>3个月。排除标准:既往接受过化疗及放疗;胃肠梗阻;消化道穿孔或出血;脑转移;对研究药物过敏;孕妇及哺乳期妇女。
本次研究经医院论理委员会批准,所有患者均签署了知情同意 两组患者一般资料比较,差异无统计学意义俨>0.05),有可比性,见表1。采用随机数字法将其分为研究组m=36)与对照组m=34)。
表1 两组患者一般资料比较
组别
性别(例) ECOC PS(例) 肝转移 肺转移 腹腔淋巴结转移 骨转移 腹水
年龄(岁)
男 女0~1分 2分 例(%) 例(%) 例(%) 例(%) 例(%)
研究组(n=36) | 56.2±10.1 | 21 | 15 | 27 | 9 | 17(47.2) | 8(22.2) | 36(100) | 4(11.1) | 3 3(91.7) |
对照组(n=34) | 55.1±12.9 | 20 | 14 | 25 | 9 | 16(47.1) | 7(20.6) | 34(100) | 3f8.81 | 31(91.2) |
1.2治疗方法
所有患者治疗前在B超定位下行腹腔穿刺,置单腔中心静脉导管引流腹水后,接受化疗,化疗方案:多西他赛(江苏恒瑞医药股份有限公司,国药准字H20020543)75 mg/m2静脉滴注;替吉奥胶囊(江苏恒瑞医药股份有限公司,国药准字H20100135)按1.25 1T12体表面积<1.5 1T12,50 mg/次,体表面积≥1.5rn2, 60 mg/次,2次ld,连续口服14 d;顺铂(江苏豪森药业集团有限公司,国药准字H20040813)40 mg/m2+生理盐水500 ml腹腔灌注,21~28 d为1个周期,共完成2—6个周期化疗。研究组在顺铂腹腔灌注前3 d联合恩度(山东先声麦得津生物制药有限公司国药准字S20050088)60 mg+生理盐水250 ml腹腔灌注,第1、3天用药。
1.3观察指标及评价标准
比较两组客观疗效、生存情况及不良反应发生情况。两组患者在每周期化疗前检查血常规、肝肾功能、心电图,首次化疗前行胸部、腹部CT扫描检查。每2个周期全面复查并按照RECIST l.0版标准评价疗效,分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和疾病进展(PD)。以CR+PR+SD计算疾病控制率(DC R)i无进展生存时间(PFS)定义为从随机分组开始至影像学检查发现肿瘤进展或者患者死亡的时间。总生存期(OS)是指从化疗开始至死亡或末次随访的时间。随访采取来院复查或电话询问方式,随访截止时间2017年6月20日。按NCI-CTC AE 3.0版评价毒副作用,分为1—5级,分别表示轻度、中度、重度,危及生命及可能导致死亡的不良反应。
1.4统计学处理
本研究数据采用SPSS 13.0统计学软件进行分析和处理,计量资料以(x+s)表示,采用£检验,客观疗效、不良反应发生率等计数资料以率(%)表示,采用,检验,Kaplan-Meier法计算无进展生存时间和总生存时间并绘制生存曲线图,P<0.05为差异有统计学意义。
2结果
2.1客观疗效
全组共完成217个周期,每例2~6个周期,研究组平均(3.5土1.5)个周期,对照组(2.7±1.4)个周期,研究组疾病控制率高于对照组,差异有统计学意义(X2=7.246.P=0.007),见表2。
表2两组患者疗效比较例(%)
组别 | CR | PR | 'SD | PD | DCR |
研究组(n=36) | 0 | 9(25.0) | 20(55.6) | 7(19.4) | 29(80.6) |
对照组m=341 | 0 | 6(17.6) | 11(32.4) | 17(50.0) | 17(50.0) |
2.2生存情况
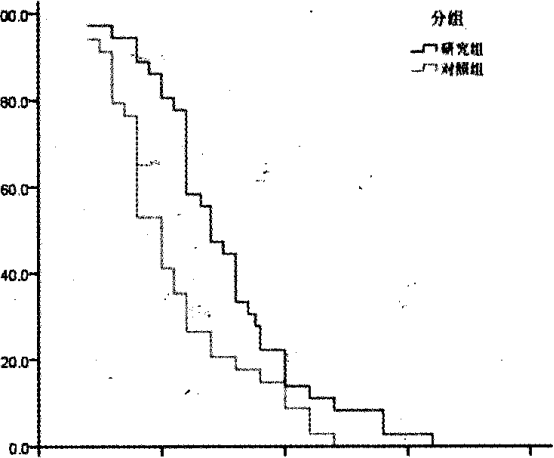
50例患者随访截止日期为2017年6月20日,研究组中位无进展生存时间(mPFS)7个月(950/oCI: 5.7,8.3),优于对照组的, 20185个月(95%CI: 4.3,5.7),差异有统计学意义(P=0.009)。研究组中位总生存时间(mOS)为10个月(95%CI: 9.2,10.8),优于对照组的8个月(95%CI: 5.7,10.2),差异有统计学意义(P=0.023),见图1、图2。
o.o s.0 100 1S 0
无进展生存期(个月J
图1 两组患者无进展生存曲线图
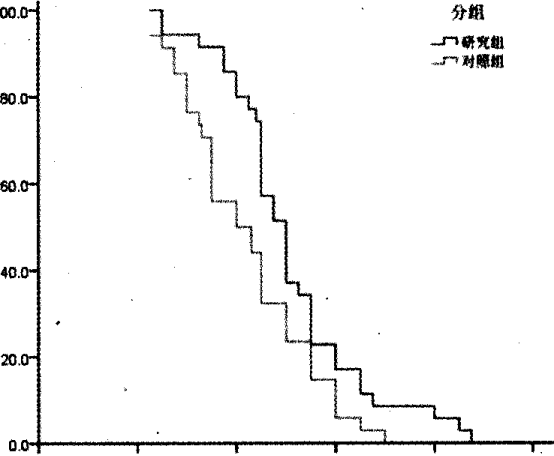
图2两组患者总生存曲线图
2.3不良反应
对本研究所有患者进行不良反应评价,常见不良反应为胃肠道反应及骨髓抑制,多数为1—2级。其中,研究组3~4级白细胞减少27.80/0,对照组为23.5%,给予粒细胞集落刺激因子药物治疗后均可较快缓解;研究组3—4级肾功能异常发生率均为8.3%,对照组为5.9%,均停止后续化疗;两组患者肠梗阻发生率较高,其中研究组肠梗阻(3~4级)发生率5.6%,对照组8.8%,未继续化疗;两组患者无化疗相关死亡。两组患者各不良反应发生率比较,差异均无统计学意义(P>0.05),见表3
表3两组患者治疗后不良反应比较例f%) | ||||||
组别 不良反应等级 | 白细胞减少 | 血小板减少 贫血 恶心/呕吐 腹泻 | 口腔溃疡 | 肝功能异常 | 肾功能异常 | 肠梗阻 |
研究组(n=3611~2级 | 14(38.9) | 8(22.2) 20(55.6) 10(27.8) 9(25.0) | 8(22.2) | 17(47.2) | 4(11.1) | 14(38.9) |
3—4级 | 10(27.8) | 0 4(11.1) 9(25.0) O | 0 | 3f8.31 | 3f8.3、 | 2f5.61 |
对照组m=34) 1~2级 | 13(38.2) | 8(23.5) 20(58.8) 8(23.5) 9(26.5) | 7(20.6) | 15(44.1) | 4(11.8) | 13(38.2) |
3~4级 | 8(23.5) | 0 4(11.8) 7(20.6) O | 0 | 2f5.91 | 2f5.91 | 3(8.8) |
3讨论
在我国胃癌确诊时大多数已属中晚期,即使行根治性手术,多数仍会复发转移,腹膜转移是常见复发部位。腹膜转移常合并大量腹水,引起患者腹胀、纳差、乏力等症状,严重影响患者生活质量,引流腹水后,导致低蛋白血症,加重营养不良、癌性恶液质的发生,加速肿瘤的进展,降低生存期。近20年,顺铂、紫杉烷类、替吉奥等多种药物用于晚期胃癌的治疗,这些药物单药有效率在200'/0左右,其中替吉奥联合顺铂化疗获得较好的效果,缓解率达41.9%[4]。但Yao等[5]报道针对腹膜转移的胃癌患者全身化疗的缓解率仅23.8%。全身化疗对腹膜转移癌疗效差,原因在于存在血一腹膜屏障,其中间皮细胞和间皮下血管网
之间的间质组织,以及腹膜癌紊乱的血供状态,导致血液内仅有少量药物能穿透此屏障进入腹膜腔,无法达到有效的血药浓度,因而腹膜腔成为全身化疗的盲区。胃癌腹膜转移患者,常规系统性全身化疗,中位生存期4—6月,预后极差[7-8]。传统观点认为胃癌腹膜转移恶性浆膜腔积液形成机制有以下:f1)淋巴管被肿瘤组织阻塞,使淋巴回流受阻;(2)肿瘤侵袭浆膜,使血管内皮细胞受损,增加血管渗透性;(3)低蛋白血症引起血浆胶体渗透压降低91。其中大量癌细胞引起腹膜毛细血管通透性增高及淋巴管阻塞、回流障碍是癌性腹水形成主要的原因。在这过程中腹腔内新生血管的形成和微血管通透性的增加起重要作用,而血管内皮生长因子是介导新生血管形成及血管通透性增加的关键调节因素。研究表明,抑制血管内皮生长因子的表达可以降低其在腹腔积液中生物活性,减少腹腔积液的形成。
恩度是1997年哈佛大学医学院Judah Folkman教授在小鼠内皮瘤中发现的内源性新生血管生成抑制因子,具有非常好的抑制动物肿瘤的效果。血管内皮抑素具有的新生血管抑制能力和对肿瘤生长抑制作用,其机制主要有以下几个方面:(1)结合内皮细胞表面的蛋白;(2)内吞进入内皮细胞;(3)影响内皮细胞的关键信号通路;(4)调节内皮细胞的基因表达谱。但单独使用血管内皮抑素很难达到显著缩小肿瘤的效果,罗永章教授发现恩度联合化疗才可明显提高治疗疗效‘叫。文献[11]报道,腹腔内灌注化疗联合全身性化疗,可以使腹腔内局部化疗药物浓度高,比单用全身化疗更有优势,腹膜内血浆浓度的曲线下面积显示腹腔灌注化疗的优势,常用于腹腔灌注的化疗药物有:紫杉醇,多西紫杉醇,5-氟脲嘧啶,顺铂等。顺铂穿透腹膜结节的能力强、化疗敏感性高,可穿透至腹膜结节表面下1~2 mm,国内学者魏红梅等”研究恩度联合顺铂治疗小鼠S180腹水瘤疗效显著,安全性好,其机制可能与恩度下调血管内皮生长因子(VEGF)和基质金属蛋白酶2(MMP-2)的表达及顺铂促进肿瘤细胞的凋亡有关。恩度联合顺铂较单药顺铂或是单药恩度疗效更高,抑制S180荷瘤小鼠腹水生成、延长存活期的作用。此外,恩度具有治疗恶性浆膜腔积液的作用,秦叔逵等的一项- 10 -全国多中心临床研究证实恩度联合顺铂治疗恶性胸腹腔积液二者有协同作用,疗效明显优于单用顺铂,联合用药组客观缓解率63%,疾病进展时间63 d。
基于上述基础及临床研究,笔者采用恩度联合顺铂腹腔灌注同时予多西他赛联合口服替吉奥双向化疗,治疗合并腹膜腔转移的晚期胃癌患者,人组患者均为晚期胃癌患者,90%以上合并腹腔积液,笔者采用腹腔置管引流腹水后,先行恩度腹腔灌注2次,第6天再联合顺铂腹腔灌注治疗,取得较好疗效,分析原因为恩度具有抑制新生血管生成作用,并可使肿瘤异常生长的血管正常化,与化疗联合有协同作用。化疗前3~6 d先使用恩度后,再行化疗可进一步提高疗效”。本研究中,联合恩度治疗有效率达81%,取得较好疗效,提示恩度持续使用可能转化为患者生存获益,值得进一步研究。
综上所述,恩度腹腔灌注联合化疗可提高临床效果,不增加明显不良反应,延长无病生存期及总生存期,可进一步进行多中心大规模临床研究,以明确胃癌腹膜转移的佳治疗方案。
参考文献
[1]汤钊猷.现代肿瘤学[M].第3版__E海:复旦大学出版社,2012:845-887.
[2]Nam H.Malignant pleural effusion: medic.al approaches for diagnosis and management[J].Tuherculosis and Respiratory Di.seases, 2014, 76(5):211-217.
[3]Lee J H, Son S Y, Lee C M,et al.Factors predicting peritoneaJ recurrence in advanced gastric cancer: implication for adjuvant intraperitonealchemotherapy.[J].Gastric Cancer, 2014, 17(3): 529-536.
[4]Weidong C,Lijun X, S-l comhined with cisplatin chemotherapy for advanCPd gastric.canc.er[J].J Canc.erRes Ther, 2016, 12(Supplement): 54-56.
[5]Yao J,Fan L,Peng C, et al.Clinical efficacy of endostar comhined with c,hemotherapy in the treatment of peritoneal carcinomatosis in gastric cancer: results from a retrospective study[Jl.Oncotarget, 2017, 8(41):70788-70797.
[6]宾业鸿,胡晓桦.胃癌腹膜转移发病机制及治疗的研究进展[J].广西医学,2016, 38(10): 1422-1426.
[7]Thomassen I,Gestel Y R V, Ramshorst B V,et aI.Peritoneal carcinomatosis of gastric origin:a population-hased study nn incidertce,survival and risk factors[J].Int J Caw.er, 2014, 134(3): 622-628.
[8]Maeda H, Kohayashi M, Sakamoto J.Evaluation and treatment nf malignant ascites secondary to gastric cancerUl.World J Castroenterol,2015, 21(39): 10936-10947.
[9]孙燕,重组人血管内皮抑制素研究与临床应用[M].北京:人民卫生出版社.2017, 140-151.
[10]陈磊,丁德权,何昌霞.重组人血管内皮抑素联合多西紫杉醇治疗胃癌恶性腹腔积液的疗效[J],中国肿瘤临床与康复,2015,10(22)1215-1217.
[11]Ishiganmi H, Yamaguchi H, Yamashita H, et al.Surgery after intraperitoneal and systemic chemotherapy for gastric cancer with peritoneal matastasis.or positive peritoneal cytology findings[J].Gastric Cancer, 2017, 20(1): 128-134.
[12]魏红梅,秦叔逵,殷晓进,等,重组人血管内皮抑素联合顺铂对小鼠腹水瘤抑制作用及其机制探讨[J]中华肿瘤防治杂志,2015,22(6): 442-446.
[13]秦叔逵,杨柳青,梁军,等,腔内应用重组人血管内皮抑制素和/或顺铂治疗恶性胸腹腔积液的前瞻性、随机对照、全国多中心Ⅲ期临床研究[J]临床肿瘤学杂志,2017, 22(3): 193-202.
[14]Jia L,Ren S,Li T,et al.Effects of Comhined Simultaneous and Sequential Endostar anrl Cisplatin Treament in a Mice Model of Castric Cancer Peritoneal Metastases[J].GastroenterolRes Pract, 2017(2): 292-384.
-
论文打印要求是什么,单面还是双面? 132985
-
ieee论文什么水平,含金量如何? 71715
-
医学硕士论文如何修改 2019.11.18 14:02
-
自血疗法联合氯雷他定治疗慢性荨麻疹的疗效观察 2019.11.18 11:26
-
Cynergy 1 064nmNd:YAG激光治疗中风险婴幼儿血管瘤疗效观察 2019.11.18 11:20
-
姜黄素及其衍生物抗菌抗炎作用研究进展 2019.11.18 10:50